ABSTRAK
Artikel ini menyajikan metode registrasi berbasis gambar fluoroskopi beserta protokol komprehensif untuk penyisipan jarum robotik dalam ablasi frekuensi radio (RFA) untuk mengobati kanker hati. Metode yang diusulkan menggunakan gambar fluoroskopi waktu nyata yang diperoleh dari sistem C-ARM dan mengintegrasikan simulasi elemen hingga (FE) terbalik untuk menghitung perintah robotik guna mengarahkan jarum secara akurat dan adaptif. Prosedur registrasi sepenuhnya otomatis dan melibatkan penyuntikan beberapa penanda radiopak ke dalam hati, yang memungkinkan registrasi anatomis yang tepat dan lokalisasi tumor yang ditargetkan. Tantangan utama yang dibahas dalam karya ini adalah integrasi registrasi berbasis gambar ini dengan simulasi biomekanik terbalik yang digunakan untuk memandu robot selama penyisipan. Kami menjelaskan bagaimana kendala registrasi dapat dipetakan ke permukaan model biomekanik untuk memastikan keselarasan yang konsisten antara data gambar dan aktuasi robotik. Dirancang agar dapat beradaptasi dengan berbagai tingkat keahlian radiologis dan dapat diterapkan di berbagai lokasi tumor, metode ini memberikan solusi yang kuat dan serbaguna untuk meningkatkan akurasi dan keamanan perawatan kanker hati minimal invasif.
1 Pendahuluan
Tumor hati ganas merupakan beban kesehatan global yang signifikan, dengan karsinoma hepatoseluler (HCC) dan metastasis hati kolorektal (CLM) menjadi jenis yang paling sering terjadi. Meskipun reseksi bedah dianggap sebagai pengobatan standar, hanya sejumlah kecil pasien yang memenuhi syarat karena lokasi tumor, luas dan distribusi lesi, penyakit ekstrahepatik, atau gangguan fungsi hati [ 1 ]. Sebagai respons terhadap tantangan klinis ini, kemajuan teknologi telah mendorong transisi yang stabil dari operasi terbuka tradisional ke intervensi dan diagnostik minimal atau non-invasif. Operasi minimal invasif (MIS) secara signifikan mengurangi risiko komplikasi, memperpendek waktu pemulihan, dan meminimalkan kerusakan jaringan.
Di antara pendekatan yang paling tidak invasif, teknik berbasis jarum telah menjadi alat penting, dengan ablasi frekuensi radio (RFA) sebagai contoh utama karena dampaknya yang minimal pada jaringan di sekitarnya.
Prosedur RFA dimulai dengan pencitraan diagnostik, baik computed tomography (CT) atau magnetic resonance imaging (MRI), untuk mengidentifikasi tumor [ 2 ]. Biasanya dilakukan dengan anestesi umum, perawatan ini melibatkan penyisipan jarum tipis ke dalam tumor. Energi frekuensi radio disalurkan melalui jarum, memanaskan dan menghancurkan sel kanker.
RFA dikenal baik karena kemampuannya untuk menargetkan tumor secara tepat sekaligus menawarkan pemulihan yang lebih cepat dan komplikasi yang lebih sedikit dibandingkan dengan operasi terbuka [ 3 ]. Durasi prosedur RFA dapat berkisar dari 30 menit hingga beberapa jam, tergantung pada pengalaman operator, protokol, ukuran tumor, dan jumlah lesi. RFA sangat efektif untuk tumor yang berukuran lebih kecil dari 3 cm, dengan angka kematian minimal dan tingkat komplikasi yang rendah.
Tantangan signifikan RFA adalah kurangnya visualisasi langsung dan akses ke organ target. Hal ini terkait dengan fakta bahwa RFA merupakan prosedur perkutan di mana jarum dimasukkan melalui kulit untuk mencapai tumor di dalam tubuh. Pencitraan medis sangat penting untuk memvisualisasikan struktur internal guna memastikan penempatan jarum yang akurat. Secara tradisional, prosedur ini dilakukan dengan menggunakan panduan ultrasonografi (USG). Meskipun ultrasonografi aman dan tidak menimbulkan ion, namun terbatas untuk memvisualisasikan tumor superfisial. Hal ini menghadirkan tantangan dalam melacak jarum secara akurat, terutama saat dimasukkan pada sudut yang curam atau jauh di dalam tubuh. Pendekatan alternatif, seperti intervensi yang dipandu CT, digunakan oleh beberapa spesialis. Dalam prosedur ini, jarum dimajukan selangkah demi selangkah, dengan pemindaian CT dosis rendah dilakukan setelah setiap penyisipan untuk menilai posisi jarum relatif terhadap tumor. Namun, metode ini sangat menantang, karena mengharuskan operator untuk memperkirakan dan menyesuaikan lintasan jarum secara mental berdasarkan umpan balik volumetrik yang tertunda—kemampuan yang biasanya hanya dikuasai oleh para ahli yang berpengalaman.
Di luar tantangan melokalisasi dan memvisualisasikan jarum dan target dengan gambar medis, menyelaraskan jarum dengan tumor secara manual adalah tugas yang rumit dan menuntut yang memerlukan keahlian klinis dan kesadaran spasial yang signifikan. Untuk mengatasi tantangan ini, sistem robotik telah diperkenalkan ke dalam radiologi intervensional. Salah satu contoh solusi komersial adalah Sistem Pemosisian Jarum DEMCON [ 4 ], yang membantu dokter dalam mencapai lintasan jarum yang tepat 1 . Namun, sebagian besar solusi robotik yang ada beroperasi dengan menyelaraskan jarum secara eksternal menggunakan lengan robotik yang memposisikan penahan jarum relatif terhadap kulit pasien. Namun, gerakan organ internal yang disebabkan oleh pernapasan menimbulkan tantangan yang signifikan. Memang, target dapat bergeser antara akuisisi gambar dan penyisipan jarum, mempersulit penempatan yang akurat dan membatasi efektivitas sistem penyelarasan eksternal murni.
Penempatan dan hipotesis : Baru-baru ini, kami mengusulkan metode panduan penyisipan jarum robotik yang memanfaatkan simulasi elemen hingga (FE) untuk mengkompensasi deformasi organ dan jarum selama prosedur [ 5 , 6 ]. Metode ini terdiri dari dua tahap utama:
- Koreksi : model FE spesifik pasien pada hati didaftarkan ke gambar medis untuk mengoreksi ketidakakuratan pemodelan. Pendaftaran ini dicapai dengan menerapkan perpindahan pada model dan menyelaraskannya dengan fitur anatomi yang dapat diamati dalam gambar untuk memastikan representasi geometri hati yang lebih akurat.
- Prediksi : model yang diperbarui kemudian digunakan untuk memprediksi perilaku organ dan posisi jarum secara lokal, dengan mempertimbangkan berbagai tindakan robotik dalam simulator. Masalah elemen hingga terbalik (iFE) dipecahkan untuk mengoptimalkan strategi kontrol dan mengarahkan jarum.
Langkah koreksi mengurangi sensitivitas terhadap ketidakpastian seperti ketidakakuratan parameter model atau asumsi kondisi batas. Menjaga konsistensi antara posisi model numerik dan struktur anatomi aktual sangatlah penting. Langkah prediksi sama pentingnya, karena penyisipan jarum adalah proses nonholonomik—yang berarti bahwa lintasan jarum, dan akibatnya kemampuan untuk mencapai tumor, bergantung pada seluruh riwayat gerakannya. Oleh karena itu, sangat penting untuk mengantisipasi gerakan struktur guna memilih lintasan optimal secara terus-menerus. Langkah ini memungkinkan pengoptimalan strategi kontrol robotik berdasarkan perilaku model numerik sebelum gerakan fisik robot dilakukan.
Metode ini telah menunjukkan kemampuan untuk mengikuti lintasan yang telah ditetapkan sebelumnya dengan presisi tinggi dalam lingkungan yang mudah bergerak dan berubah bentuk, sehingga memungkinkan penyisipan jarum yang akurat. Akan tetapi, percobaan sebelumnya dilakukan dalam pengaturan laboratorium yang disederhanakan, menggunakan penanda 3D yang ditempatkan langsung pada permukaan model untuk registrasi (koreksi). Pendekatan ini tidak layak dalam konteks intervensi perkutan, karena akan memerlukan pembukaan rongga perut.
Dalam artikel ini, kami mengandalkan protokol eksperimental untuk mendaftarkan model numerik yang terinspirasi oleh sistem CyberKnife [ 7 ], yang menggunakan fluoroskopi untuk ablasi tumor dengan sinar radiasi dan fiducial emas yang dimasukkan secara perkutan untuk pelacakan. Tidak seperti pendekatan CyberKnife standar, metode kami memanfaatkan model FE untuk memperhitungkan deformasi hati dengan melacak gerakan penanda fiducial dalam gambar fluoroskopi proyektif 2D. Kami menangani masalah registrasi nonrigid 2D/3D dan menguji metode tersebut dalam simulasi dan eksperimen hewan.
Mengenai kemudi jarum robotik, meskipun penanda memungkinkan registrasi model, penanda tersebut cenderung membatasi deformasinya, yang secara efektif “memperkeras” model secara artifisial. Masalah ini sangat penting karena penanda tersebut terletak di dalam volume organ dan mungkin terletak dekat dengan lintasan jarum. Hal ini secara langsung memengaruhi medan deformasi di wilayah yang diinginkan selama langkah simulasi terbalik. Pengerasan artifisial tersebut mendistorsi perilaku organ yang diprediksi, yang pada akhirnya mengurangi keakuratan strategi kontrol robotik yang diperoleh selama fase prediksi.
Kontribusi utama dari karya ini adalah perumusan ulang kendala registrasi dengan memindahkannya dari penanda internal ke permukaan organ. Pendekatan ini mengurangi distorsi perilaku organ yang diprediksi dalam volume—terutama di sekitar lintasan jarum—sambil mempertahankan fleksibilitas yang cukup dalam model untuk menghitung strategi kontrol robotik yang akurat untuk panduan jarum. Pada saat yang sama, ia mempertahankan registrasi model yang andal menggunakan gambar fluoroskopik.
2 Karya Terkait
2.1 Registrasi Gambar yang Dapat Dideformasi
Registrasi yang dapat dideformasi antara modalitas pencitraan 2D dan 3D telah lama menjadi tugas yang menantang dalam analisis citra medis. Hal ini terutama berlaku untuk organ seperti hati, yang mengalami gerakan nonrigid dan perubahan bentuk yang signifikan. Berbagai metode telah dikembangkan untuk mengatasi masalah ini, termasuk teknik yang bergantung pada intensitas citra dan teknik yang didasarkan pada fitur anatomi yang khas.
Pekerjaan awal difokuskan pada registrasi 2D-3D yang kaku atau afin, Maes et al. [ 8 ] telah menunjukkan keefektifan di seluruh skenario pencitraan multimoda. Teknik berbasis fitur mengekstraksi landmark atau kontur anatomi yang menonjol dan digunakan secara luas untuk registrasi organ yang kaku dan afin. Algoritma setan Maxwell dalam [ 9 ] dan registrasi berbasis B-spline [ 10 ] telah menunjukkan kinerja yang kuat dalam menyelaraskan organ jaringan lunak, khususnya dalam pemindaian MRI dan CT. Namun, meskipun efisien secara komputasi, metode ini gagal menangkap deformasi kompleks yang khas dari jaringan lunak. Untuk mengatasi keterbatasan ini, para peneliti memperkenalkan model biomekanik dan model bentuk statistik. Misalnya, Lange et al. [ 11 ] mengusulkan pendekatan registrasi kaku dan tidak kaku berbasis intensitas. Metode informasi timbal balik dan korelasi silang yang dikembangkan oleh Rucker et al. [ 12 ] menyelaraskan model hati biomekanik (dibangun dari gambar pra operasi) dengan data geometrik yang tidak lengkap yang mewakili lokasi daerah hati yang jarang yang dikumpulkan secara intraoperatif.
Pembelajaran mendalam telah memajukan bidang ini secara signifikan, memungkinkan metode registrasi berbasis data yang lebih cepat dan seringkali lebih tangguh. Sokooti dkk. [ 13 ] memperkenalkan pendekatan berbasis CNN untuk memperkirakan medan deformasi padat dari gambar berpasangan. Pendekatan seperti VoxelMorph [ 14 ] menggunakan jaringan saraf konvolusional untuk memprediksi medan perpindahan padat, yang memungkinkan registrasi waktu nyata tanpa pengoptimalan berulang. Metode ini telah diperluas ke berbagai organ, termasuk otak, paru-paru, dan hati, dengan hasil yang menjanjikan. Pendekatan pembelajaran mendalam lainnya diperkenalkan untuk mengatasi tantangan registrasi gambar ultrasonografi 2D dengan gambar CT/MRI 3D selama prosedur ablasi tumor hati dan telah dikembangkan oleh Wei dkk. [ 15 ]. Penelitian mereka menekankan pentingnya registrasi gambar yang akurat untuk meningkatkan penyelarasan pasien selama operasi. Ini juga memperkenalkan pendekatan pembelajaran mendalam yang ditujukan untuk membuat registrasi lebih tepat.
Dalam registrasi berbasis penanda, metode REALMS [ 16 ] memperkenalkan pendekatan pembelajaran metrik lokal untuk registrasi deformable 2D/3D, khususnya menargetkan jaringan lunak abdomen yang terpengaruh oleh gerakan pernapasan. Dengan berfokus pada daerah di sekitar penanda fiducial yang ditanamkan. Tascón-Vidarte dkk. [ 17 ] mengevaluasi keakuratan registrasi gambar deformable berbasis intensitas (DIR) untuk tumor hati selama gerakan pernapasan. Penanda fiducial emas yang ditanamkan digunakan sebagai referensi untuk menilai keakuratan registrasi. Kesalahan registrasi rata-rata kurang dari 1,6 mm, yang menunjukkan bahwa DIR berbasis intensitas dapat memperkirakan posisi tumor di hati selama siklus pernapasan dengan andal.
Namun, metode-metode ini tidak bersifat real-time atau memiliki batasan spasial. Adagolodjo et al. [ 18 ] memperkenalkan metode registrasi yang menggunakan penanda untuk mengembangkan sistem augmented reality (AR) untuk memfasilitasi operasi hati terbuka.
Mengambil keuntungan dari keamanan dalam penempatan penanda fiducial sebelum radioterapi tubuh stereotactic untuk tumor hati ganas menggunakan Cyberknife [ 19 ], kami memperkenalkan penanda sebagai titik referensi tetapi hanya menggunakan satu sumber sinar-X sebagai modalitas pencitraan, berbeda dari Cyberknife, yang memiliki dua sumber sinar-X yang dipasang di langit-langit atau dinding pada sudut 90 derajat satu sama lain.
Dalam karya ini, kami memperluas pendekatan menggunakan data medis yang kompatibel dengan prosedur perkutan, yang mengharuskan perut tetap tertutup selama intervensi. Salah satu tantangan utama adalah memperoleh gambar dengan bidang pandang yang luas sekaligus memastikan akuisisi gambar yang cepat. Kami berasumsi penanda ditempatkan secara perkutan di hati sebelum prosedur dan tidak bergeser dari posisi yang dimasukkan. Meskipun langkah ini bersifat invasif, kami menunjukkan bahwa hal ini memungkinkan presisi tinggi dalam panduan penyisipan jarum.
2.2 Bantuan Robotik dalam Terapi Ablasi Perkutan
Panduan robotik untuk ablasi telah berkembang secara signifikan selama dekade terakhir, didorong oleh kebutuhan akan peningkatan presisi, keamanan, dan konsistensi dalam penargetan tumor.
Sistem robotik terutama difokuskan pada posisi jarum yang tepat, yang memungkinkan dokter untuk memandu jarum di sepanjang lintasan yang telah ditentukan sebelumnya untuk menargetkan tumor secara akurat dan konsisten [ 20 , 21 ]. Song et al. [ 22 ] mengusulkan mekanisme RCM cincin ganda untuk panduan jarum robotik dalam intervensi hati yang dipandu MRI. Namun, percobaan tersebut dilakukan tanpa gerakan pasien melalui gerakan pernapasan dan tidak ada pembengkokan jarum yang dipertimbangkan. Banyak sistem robotik, seperti platform MAXIO dan ROBIO-EX, menggunakan lengan yang diartikulasikan dan penahan jarum tetap untuk memastikan penyelarasan jarum yang akurat, mengurangi ketergantungan pada pengalaman operator dan ketangkasan manual [ 23 ]. Baru-baru ini, platform robotik mulai menggabungkan strategi kontrol tingkat lanjut dan kemampuan otonom. Sistem seperti robot Epione dengan enam derajat kebebasan untuk menyelaraskan jarum secara akurat dan memfasilitasi jalur penyisipan yang kompleks, memungkinkan navigasi yang aman di sekitar struktur anatomi yang kritis [ 24 ]. Sistem biopsi robotik kolaboratif dalam [ 25 ] mengintegrasikan panduan lintasan dengan umpan balik haptik dari gaya ujung jarum untuk meningkatkan akurasi penempatan jarum. Pendekatan ini dimulai dengan fase perencanaan, memanfaatkan pencitraan CT untuk menentukan lintasan penyisipan yang optimal, diikuti oleh robot yang disesuaikan yang menyelaraskan jarum. Sistem ini menggunakan jarum pintar dengan sensor gaya optik, yang memungkinkan pemantauan gaya yang bekerja pada ujung jarum secara real-time melalui tomografi koherensi optik (OCT) dan algoritma pembelajaran mendalam. Hungr dkk. [ 26 ] memperkenalkan robot tusuk cahaya yang dirancang untuk prosedur toraks dan abdominopelvis di bawah panduan CT dan MRI, yang menekankan akurasi penargetan yang ditingkatkan dan waktu prosedur yang berkurang. Ini menyoroti berbagai arsitektur dan tingkat otomatisasi robot yang dirancang untuk pengaturan yang berbeda sambil berbagi ketergantungan pada pencitraan medis untuk panduan. Hiraki dkk. [ 27 ] menyajikan sistem Zerobot, robot yang dikendalikan dari jarak jauh untuk penyisipan jarum yang dipandu CT, yang memamerkan keunggulannya dibandingkan prosedur manual, seperti berkurangnya kelelahan dokter dan paparan radiasi, posisi jarum yang stabil, dan otomatisasi. Artikel ini membahas potensi uji klinis dan komersialisasi, yang menandai kemajuan signifikan dalam intervensi yang dipandu CT. [ 28 ] merinci sistem presisi untuk penempatan jarum yang dipandu CT di toraks dan perut, mencapai kesalahan penempatan rata-rata dalam persyaratan klinis. Komponen sistem tersebut mencakup sistem registrasi, sistem penggerak, dan tautan struktural untuk meminimalkan kepatuhan, yang menunjukkan harapan untuk aplikasi klinis. Pfeil dkk. [ 29] mengusulkan sistem robotik yang dipasang di meja yang terintegrasi dengan computed tomography cone-beam (CBCT) untuk memudahkan panduan jarum tanpa memerlukan klem ekstensi dan secara signifikan mengurangi paparan radiasi pada tangan operator. Secara khusus, sistem robotik iSYS CT/CBCT adalah platform yang dipasang di meja dengan empat DOF. Sistem ini menggunakan dua tahap datar penerjemahan paralel (sering digambarkan sebagai konfigurasi ‘sandwich’), yang dikendalikan dari jarak jauh melalui joystick. Desain ini memungkinkan posisi jarum yang akurat selama intervensi yang dipandu dari jarak jauh di bawah pencitraan CT, CBCT, atau fluoroskopi, yang secara substansial menurunkan paparan radiasi bagi personel medis yang terlibat.
Namun, robot yang dipasang di lantai tersebut mengasumsikan pasien tetap diam; mereka tidak menyesuaikan diri secara dinamis dengan gerakan organ. Selain itu, integrasi dengan pencitraan (CT) memerlukan kalibrasi yang cermat dan menambah beban pada ruang prosedur. Robot yang dipasang pada pasien yang lebih baru 2 bertujuan untuk mengatasi beberapa tantangan integrasi ini dengan menempel langsung ke tubuh pasien. Meskipun fluoroskopi CT (tampilan irisan terpilih yang mendekati waktu nyata pada 1–8 fps) membantu dalam memandu jarum, gerakan jarum yang cepat masih dapat melampaui kecepatan tampilan. Untuk mengatasi masalah ini, penelitian kami bertujuan untuk mengembangkan registrasi fluoroskopi 2D/3D waktu nyata untuk algoritma pengarah jarum yang terbukti pada organ yang dapat dideformasi selama respirasi sehingga robot 6-dofs dapat melakukan pengarahan jarum dengan waktu intervensi yang berkurang dan akurasi yang lebih baik.
3 Pemodelan dan Simulasi
Pada bagian ini, kami menyajikan kerangka kerja numerik yang memungkinkan simulasi model jarum dan jaringan, beserta interaksi dan kendala yang diperlukan untuk mensimulasikan penyisipan jarum dan registrasi model.
3.1 Model Jarum dan Jaringan
Formulasi korotasional hukum Hooke digunakan untuk memodelkan volume hati menggunakan elemen tetrahedral linier [ 30 ]. Formulasi korotasional memungkinkan representasi respons hati terhadap gaya eksternal yang lebih akurat dengan memisahkan rotasi benda tegar dari deformasi material. Metode ini secara efisien menangkap nonlinieritas geometri yang disebabkan oleh rotasi besar tanpa mengorbankan efisiensi komputasi, sehingga sangat cocok untuk simulasi waktu nyata dalam aplikasi medis. Penggunaan elemen tetrahedral linier memastikan keseimbangan antara biaya komputasi dan kemampuan untuk memodelkan deformasi kompleks jaringan hati.
Jarum, di sisi lain, dimodelkan secara terpisah menggunakan teori balok Timoshenko, yang memperhitungkan deformasi tekukan dan geser. Teori ini khususnya berguna untuk mensimulasikan perilaku mekanis struktur ramping seperti jarum, di mana baik tekukan maupun deformasi aksial signifikan. Jarum didiskritisasi menjadi elemen balok satu dimensi, dengan setiap simpul dalam jaring elemen hingga memiliki enam derajat kebebasan (DOF). DOF ini mencakup tiga gerakan translasi dan tiga gerakan rotasi, yang memungkinkan representasi komprehensif dari perilaku jarum selama penyisipan.
3.2 Resolusi Kendala Menggunakan Pengganda Lagrange
Karena model organ dan jarum tidak memiliki derajat kebebasan (DOF) yang sama, interaksi antara benda yang dapat dideformasi dan kendala perpindahan ditangani menggunakan pengganda Lagrange [ 31 ]. Kendala tambahan yang diperkenalkan dalam sistem harus dipenuhi pada akhir setiap langkah waktu, karena ini penting untuk menjaga jarum di sepanjang lintasan yang dimaksudkan dan untuk mensimulasikan fenomena penting secara akurat, seperti gesekan antara struktur selama penyisipan [ 32 ]. Ketika beberapa objek yang dapat dideformasi berinteraksi, masalah mekanis diformulasikan sebagai sistem Karush–Kuhn–Tucker (KKT):

3.3 Registrasi 2D/3D untuk Needle Steering
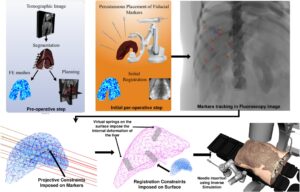
Protokol dimulai dengan penempatan penanda fiducial internal (lihat Gambar 2 ). Seperti yang dijelaskan dalam penelitian sebelumnya [ 35 ], fiducial ini—biasanya terbuat dari emas—terlihat secara radiografis dan ditempatkan di dalam atau di sekitar lesi di bawah panduan gambar oleh ahli radiologi intervensional. Peran mereka adalah untuk berfungsi sebagai landmark yang dapat diandalkan untuk pelacakan lesi selama perawatan, terutama pada adanya gerakan pernapasan atau pergeseran organ internal. Dalam protokol kami, fiducial dimasukkan secara perkutan ke dalam hati tanpa kendala ketat pada lokasi intrahepatik yang tepat, selama mereka dipisahkan secara spasial untuk memungkinkan identifikasi individu yang jelas pada pencitraan dan tetap stabil pada posisinya selama intervensi. Dalam penelitian ini, kami secara khusus mengevaluasi pengaruh jumlah fiducial pada akurasi pelacakan.
Untuk menggunakan penanda secara efektif, penting untuk menetapkan korespondensi yang tepat antara lokasi anatomisnya di dalam hati dan representasi spasial 3D-nya. Untuk tujuan ini, kami memanfaatkan sistem pencitraan Artis Zeeog yang tersedia di lembaga kami (IHU Strasbourg), yang memungkinkan perolehan beberapa tampilan fluoroskopi dan rekonstruksi volume 3D berikutnya untuk menetapkan korespondensi spasial ini.
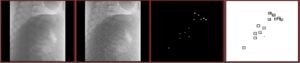
Selama prosedur, gambar fluoroskopik diambil pada beberapa bingkai per detik. Alur kerja dimulai dengan pengambilan gambar mentah, diikuti dengan penerapan filter praproses yang dirancang untuk meningkatkan dan mengisolasi fitur visual utama yang diperlukan untuk pelacakan yang kuat (lihat Gambar 1 ). Langkah-langkah ini mencakup filter penajaman untuk menekankan tepi dan detail struktural yang halus, dan filter ambang batas untuk mengubah gambar menjadi format biner, yang menyederhanakan deteksi penanda. Filter wilayah minat (ROI)—seperti kotak pembatas atau masker khusus—kemudian diterapkan untuk membatasi analisis ke area anatomi yang relevan. Untuk pelacakan gerakan, kami menggunakan algoritme aliran optik OpenCV, dengan parameter yang dioptimalkan secara manual untuk memastikan ketepatan pelacakan yang tinggi. Algoritme ini memperkirakan perpindahan penanda antara bingkai yang berurutan, yang memungkinkan rekonstruksi lintasan gerakannya dari waktu ke waktu. Dengan mengintegrasikan teknik-teknik ini, kami mencapai pelacakan yang akurat dan konsisten di seluruh rangkaian video, yang memungkinkan analisis terperinci tentang perilaku dinamis penanda. Pada akhirnya, proses ini memungkinkan kami untuk menentukan posisi setiap penanda fiducial secara andal di setiap gambar fluoroskopik 2D.

4 Pemasangan Jarum Otomatis Menggunakan Elemen Hingga Terbalik
Masalah kemudi jarum robot diformulasikan sebagai masalah minimisasi fungsi nonlinier [ 5 , 6 , 37 ]:

- Sasaran lintasan : batasan ini memastikan bahwa ujung jarum mengikuti lintasan yang telah ditetapkan sebelumnya yang beradaptasi dengan deformasi dan gerakan organ. Batasan ini meminimalkan jarak antara ujung jarum dan titik target yang bergerak di lintasan.
- Sasaran orientasi jarum : dua batasan sudut diberlakukan: yang pertama menyelaraskan ujung jarum dengan garis singgung lintasan, dan yang kedua menyelaraskan dasar jarum (end-effector robot) dengan vektor yang mengarah ke titik masuk. Batasan ini mempertahankan orientasi penyisipan yang benar.
- Sasaran titik masuk : menggunakan pendekatan pusat gerak jarak jauh (RCM), kendala ini memastikan bahwa titik masuk jarum pada kulit tetap stabil. Pada setiap langkah waktu, posisi awal diproyeksikan ke poros jarum untuk meminimalkan deviasi.
Tujuan-tujuan ini dipecahkan bersama-sama dalam masalah optimasi multiobjektif menggunakan metode elemen hingga terbalik. Karena sifat interaksi jarum-jaringan yang nonlinier, metode elemen hingga terbalik (iFE) [ 38 ] digunakan untuk menghitung pose efektor akhir robot. Metode ini memecahkan masalah minimisasi pada setiap langkah waktu. Ekspansi Taylor orde pertama diterapkan:

4.1 Registrasi Hati dengan Batasan Registrasi Transfer pada Permukaan
Perbedaan utama pendekatan kami dibandingkan dengan pekerjaan sebelumnya adalah penggunaan penanda internal untuk registrasi model. Dalam penelitian sebelumnya [ 5 , 6 , 37 ], penanda fiducial biasanya ditempatkan pada permukaan model organ—strategi yang tidak berlaku dalam konteks prosedur perkutan. Dalam protokol kami, penanda dimasukkan langsung ke hati melalui akses perkutan, menjadikan fiducial internal pilihan yang lebih tepat dan layak secara klinis. Namun, jika penanda ini diposisikan terlalu dekat dengan jalur penyisipan jarum, kendala registrasi yang diterapkan pada titik-titik ini dapat secara signifikan memengaruhi deformasi model. Secara khusus, kendala yang diberlakukan mencegah gerakan apa pun di sepanjang garis pandang yang ditentukan oleh proyeksi fluoroskopik. Akibatnya, model menjadi terlalu dibatasi di wilayah tersebut, yang dapat menghambat kemampuannya untuk secara akurat mensimulasikan perilaku jaringan di dekat jarum, terutama dalam konteks panduan dinamis.
Ketika penanda ditempatkan cukup jauh dari ujung jarum, pengerasan buatan ini memiliki dampak kecil pada perhitungan gradien
. Namun jika penanda terletak di dekat lintasan, tidak ada gerakan relatif antara jarum dan jaringan yang dapat ditangkap, dan persamaan ( 1 ) akan menghasilkan Jacobian nol. Secara lebih luas, dalam kasus kendala proyektif, model tersebut menunjukkan mobilitas anisotropik: model tersebut jauh lebih fleksibel di sepanjang garis proyeksi—di mana tidak ada kendala registrasi yang diberlakukan—daripada di bidang gambar, di mana perpindahan diberlakukan. Hal ini memperkenalkan bias yang signifikan dalam Jacobian, membatasi kemampuan pengoptimal untuk menyesuaikan strategi kontrol secara lokal, dan dalam beberapa kasus, dapat mencegah panduan jarum yang efektif sama sekali.
Dalam artikel ini, kami memperkenalkan langkah perantara di mana model organ pertama kali didaftarkan ke penanda fiducial internal tanpa mempertimbangkan interaksi jarum-jaringan atau kontrol robotik (lihat Gambar 2 ). Langkah ini melibatkan simulasi pendaftaran 2D/3D murni yang hanya berdasarkan pada posisi penanda. Setelah keseimbangan mekanis tercapai, kami mengekstrak permukaan model yang didaftarkan, yang dilambangkan sebagai
.
Hasilnya, selama langkah simulasi terbalik, tidak ada perpindahan yang diberlakukan dalam volume model—hanya permukaannya yang dibatasi. Namun, karena jarum dimasukkan jauh ke dalam volume, hubungan antara jarum dan jaringan sebagian besar tidak terpengaruh oleh batasan permukaan. Pendekatan ini memungkinkan simulasi deformasi lokal di sekitar jarum, terlepas dari distribusi spasial penanda internal. Akibatnya, pendekatan ini memungkinkan penghitungan gradien yang lebih akurat dan kurang bias, yang mengarah pada peningkatan kinerja strategi panduan jarum kami.
5 Percobaan dan Hasil
Dalam studi ini, kami menilai kinerja metode yang kami usulkan di berbagai pengaturan. Awalnya, kami mengevaluasi algoritme pelacakan menggunakan gambar fluoroskopik nyata dari hati babi yang sedang bernapas, di mana penanda fiducial ditempatkan untuk memfasilitasi proses registrasi. Selanjutnya, kami menerapkan metode kendali pengarahan jarum kami ke data dari hati manusia, dengan fokus pada penyisipan robotik dan mengevaluasi dampak teknik registrasi. Metode registrasi dan penyisipan robotik dinilai secara eksklusif dalam konteks numerik, menggunakan data khusus pasien untuk evaluasi ini. Hasilnya menunjukkan bahwa pendekatan kami secara efektif beradaptasi dengan kondisi dunia nyata, memastikan panduan jarum yang tepat dan secara signifikan meningkatkan akurasi keseluruhan proses penyisipan.
5.1 Pelacakan Penanda dalam Gambar Fluoroskopi
Dalam penelitian ini, kami menanamkan 12 penanda fiducial secara perkutan ke dalam tubuh babi untuk memudahkan pelacakan dan analisis (Gambar 1 ). Gambar fluoroskopi kemudian diambil menggunakan sistem Artis Zeego. Pengambilan gambar dilakukan selama beberapa siklus pernapasan untuk menangkap gerakan dinamis selama bernapas. Data ini dikumpulkan sebagai bagian dari protokol yang dilakukan di IHU Strasbourg, dengan mematuhi pedoman dan peraturan etika yang berlaku saat itu.
![]()
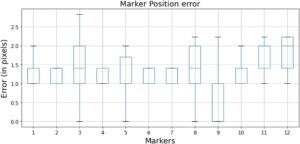
Untuk setiap gambar dalam urutan tersebut, penanda diidentifikasi secara manual, yang berarti bahwa penanda tersebut disegmentasikan secara manual di setiap gambar untuk berfungsi sebagai kebenaran dasar. Proses segmentasi dilakukan dua kali di seluruh urutan, dan rata-rata posisi yang disegmentasi digunakan sebagai kebenaran dasar untuk perbandingan. Nilai kebenaran dasar ini kemudian dibandingkan dengan posisi penanda 2D yang sesuai yang diperkirakan menggunakan teknik aliran optik. Seperti yang diilustrasikan dalam Gambar 3 , metode pelacakan kami mencapai margin kesalahan sekitar 1–2 piksel.
5.2 Pengarahan Jarum pada Model Hati Manusia
Pada bagian ini, kami menyajikan penerapan teknik pengarahan jarum pada model hati manusia, dengan menekankan tantangan dan strategi yang diperlukan untuk mencapai penyisipan jarum yang tepat ke dalam jaringan lunak. Hati telah disegmentasi oleh ahli radiologi menjadi dua zona berbeda, masing-masing memiliki tingkat kesulitan yang berbeda untuk prosedur penyisipan jarum (Gambar 4 ).
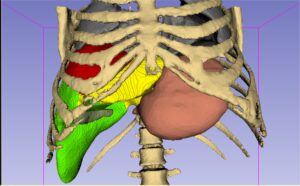
Ahli kami kemudian mendefinisikan dua jalur penyisipan jarum untuk setiap area target. Lintasan pertama relatif mudah (digambarkan dalam warna merah muda), yang memungkinkan penyisipan jarum langsung untuk menargetkan tumor di dalam hati (pendekatan dalam bidang) (Gambar 5a ). Jalur ini biasanya memerlukan manuver yang kurang rumit, dengan jarum dimasukkan pada sudut hampir tegak lurus (sekitar 90 derajat) ke permukaan tubuh, yang memastikan jalur yang mudah. Sebaliknya, lintasan yang rumit (ditunjukkan dengan warna biru) menuntut penyisipan jarum yang hati-hati dan miring untuk menghindari struktur kritis, seperti paru-paru, yang membuat prosedur lebih rumit dan memerlukan presisi yang lebih tinggi. Karena dalam pencitraan CT, jarum dalam kasus ini sering muncul sebagai titik tunggal (lihat Gambar 5b ) atau segmen pendek karena perspektif pencitraan yang terbatas (pendekatan di luar bidang).
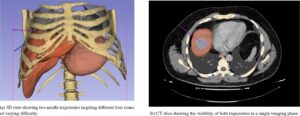
5.2.1 Evaluasi Akurasi Registrasi Berbasis Penanda
Untuk mengevaluasi keakuratan proses registrasi, kami menerapkan pendekatan berbasis penanda di mana sembilan penanda fiducial didistribusikan secara seragam dalam model anatomi. Penanda ini berfungsi sebagai titik referensi untuk menyelaraskan model. Simulasi pelengkap, yang disebut sebagai “simulasi langsung”, dari gerakan hati saat bernapas dibuat, termasuk interaksi dengan organ di sekitarnya seperti lambung dan usus. Simulasi langsung berfungsi sebagai dasar kebenaran untuk menilai keakuratan registrasi dan posisi jarum.
Selain itu, kerangka simulasi kami mencakup mesin rendering sinar-X yang secara fisik realistis yang memodelkan redaman sinar-X melalui kepadatan jaringan yang berbeda [ 39 ] (Gambar 2 ). Hal ini memungkinkan kami untuk menghasilkan gambar fluoroskopi sintetis yang sangat mirip dengan gambar fluoroskopi asli. Penyerapan sinar-X yang disimulasikan oleh berbagai jaringan dan material dalam model memastikan bahwa tampilan visual dari penanda dan struktur anatomi realistis dan sebanding dengan pencitraan klinis. Selama proses registrasi, sistem membandingkan posisi penanda yang terlihat dalam gambar simulasi dengan koordinat 3D yang diketahui dalam model langsung. Dengan menerapkan metode pelacakan yang dijelaskan sebelumnya, kami mencapai kesalahan piksel yang sebanding dengan yang diamati dalam gambar sinar-X asli yang diperoleh dari hati babi.

5.2.2 Evaluasi Kuantitatif Akurasi Penusukan Jarum

Hasil pada Gambar 6 menunjukkan bahwa dengan menerapkan kendala proyektif pada penanda di dalam hati, registrasi menghasilkan kesalahan yang lebih besar pada posisi jarum daripada mentransfer kendala ke permukaan. Dengan registrasi permukaan, semua kombinasi kesulitan lintasan dan jumlah penanda berhasil menargetkan tumor pada akhirnya, yang secara meyakinkan menunjukkan keefektifan metode tersebut. Kesalahan rata-rata tumbuh dari lintasan yang mudah ke lintasan yang sulit, dan dari metode mentransfer kendala ke permukaan ke lintasan di mana kendala diberlakukan pada penanda.

Hasil pada Gambar 7 menunjukkan penyisipan sepanjang lintasan menuju target mudah dan sulit, dengan panjang masing-masing 4,5 dan 7 cm. Seiring dengan penyisipan, kesalahan memiliki bentuk sinusoidal karena pernapasan. Pengamatan ini menyoroti dampak faktor pernapasan pada keakuratan penyisipan jarum, yang menunjukkan perlunya strategi kontrol adaptif untuk memperhitungkan variasi tersebut. Namun, ketika target lintasan mencapai akhir, kesalahannya kurang dari 2,5 mm, yang menunjukkan efektivitas keseluruhan metode kami. Seperti yang diharapkan, dengan pengurangan penanda, kesalahan penanda memiliki interval 3,9 hingga 7,5 mm.

6. Pembahasan dan Kesimpulan
Pelacakan penanda kami divalidasi menggunakan gambar sinar-X asli. Sebaliknya, eksperimen registrasi dilakukan dengan gambar sinar-X sintetis, yang memungkinkan manipulasi organ yang dapat dideformasi dalam lingkungan simulasi dan mengonfirmasi pengulangan. Sebuah metode yang memanfaatkan gambar fluoroskopi telah diperkenalkan untuk mencapai registrasi organ waktu nyata selama respirasi. Pendekatan ini kompatibel dengan algoritma pengarah jarum yang sudah mapan yang digunakan dalam organ yang dapat dideformasi, menggunakan loop simulasi terbalik yang dioptimalkan. Teknik-teknik ini memungkinkan kami untuk memandu jarum dengan perangkat pencitraan waktu nyata seperti fluoroskopi, memastikan registrasi organ yang tepat dan mematuhi rekomendasi prosedur ablasi frekuensi radio (RFA). Metode ini dievaluasi dalam kerangka simulasi realistis yang dibuat dari data pemindaian CT manusia, yang menunjukkan pengulangannya.
Alur kerja yang diusulkan, meskipun invasif, dirancang dengan mengutamakan keselamatan pasien sebagai prioritas utama. Penempatan penanda di dalam hati diperlukan, suatu proses yang terbukti aman dari pengalaman Cyberknife. Manfaat metode kami, termasuk peningkatan signifikan dalam presisi penyisipan jarum dan waktu pengarahan yang minimal, menanamkan keyakinan pada potensi keberhasilan prosedur. Lebih jauh, metode yang kami usulkan memungkinkan ahli radiologi untuk melakukan teleoperasi dari jarak jauh, yang menyediakan langkah-langkah keamanan tambahan. Terakhir, penyisipan jarum dapat menargetkan tumor di dalam zona keras (warna merah pada Gambar 4 ).
Pekerjaan kami selanjutnya akan menerapkan metode pendaftaran hati dengan platform eksperimental menggunakan Zeego C-Arm dengan mayat babi. Selanjutnya, penyisipan jarum akan dilakukan menggunakan sistem robotik. Pengaturan langkah-langkah intraoperatif direpresentasikan dalam Gambar 8 , di mana ahli radiologi dapat mengawasi proses ablasi tanpa terpapar radiasi.